文章目录[隐藏]
- Th1和Th2亚群检测
- th1和th2细胞因子
- 联科生物Th1/Th2/Th17检测产品列表
- Human Th1/Th2/Th17 Staining Kit 人Th1/Th2/Th17染色试剂盒
- 定制Human Th1/Th2/Th17 Staining Kit II
- Human Th1/Th2 Staining Kit 人 Th1/Th2 染色试剂盒
- Human Th17 Staining Kit 人 Th17 染色试剂盒
- Mouse Th1/Th2 Staining Kit 小鼠辅助性Th1/Th2细胞检测试剂盒
- Mouse Th17 Staining Kit 小鼠辅助性Th17细胞检测试剂盒
- FoxP3/Transcription Factor Staining Buffer Kit
- 联科生物Treg检测产品列表
- Human Regulatory T Cell Staining Kit 人调节性T细胞染色试剂盒
- Mouse Regulatory T Cell Staining Kit小鼠调节性T细胞染色试剂盒
- FoxP3/Transcription Factor Staining Buffer Kit
- 试剂盒组分(以小鼠Th1/Th2检测为例)
- 样本采集及制备
- 刺激及染色
- 流式检测
- 结果示例
Th1和Th2亚群检测
通常所说的Th1、Th2是指在各种生理与病理条件下有能力分化为Th1、Th2的辅助性T细胞 (严格意义上是 Th0)。静息状态 (未受任何刺激,如人的正常生理状态)下,Th0分化为Th1、Th2的能力非常弱;当受到外界因素(如刺激素、病原体等)刺激,Th0即会向Th1、Th2等Th细胞分化,此时,通过检测分泌的细胞因子(如IFN-γ、IL-4等)实现对各类Th细胞的检测。正常情况下机体中Th1和Th2处于相对平衡的状态,当这种平衡打破时可能引起多种疾病的发生,如肿瘤、自身免疫性疾病等。

th1和th2细胞因子
Th1/Th2可分泌多种细胞因子,参与不同免疫应答:
- Th1:分泌 IFN-γ、IL-2、TNF-α 等细胞因子,主要介导细胞免疫应答,调节细胞毒性T细胞分化和参与迟发型超敏反应;
- Th2:分泌 IL-4、IL-10、IL-13 等细胞因子,主要介导体液免疫,促进B细胞增殖、分化和产生抗体。
联科生物Th1/Th2/Th17检测产品列表
-


- KTH001 2 Citations
- Th/Treg分型检测试剂盒
Human Th1/Th2/Th17 Staining Kit 人Th1/Th2/Th17染色试剂盒
- ¥3,200.00 – ¥12,000.00
-


- KTH002
- Th/Treg分型检测试剂盒
定制Human Th1/Th2/Th17 Staining Kit II
- ¥3,200.00
-


- KTH101
- Th/Treg分型检测试剂盒
Human Th1/Th2 Staining Kit 人 Th1/Th2 染色试剂盒
- ¥2,550.00 – ¥9,580.00
-


- KTH117 3 Citations
- Th/Treg分型检测试剂盒
Human Th17 Staining Kit 人 Th17 染色试剂盒
- ¥2,680.00 – ¥10,050.00
-


- KTH201 16 Citations
- Th/Treg分型检测试剂盒
Mouse Th1/Th2 Staining Kit 小鼠辅助性Th1/Th2细胞检测试剂盒
- ¥1,850.00 – ¥6,940.00
-


- KTH217 19 Citations
- Th/Treg分型检测试剂盒
Mouse Th17 Staining Kit 小鼠辅助性Th17细胞检测试剂盒
- ¥1,940.00 – ¥7,290.00
-


- IC001 15 Citations
- 固定破膜剂
FoxP3/Transcription Factor Staining Buffer Kit
- ¥320.00 – ¥1,140.00
联科生物Treg检测产品列表
-


- KTR101 4 Citations
- Th/Treg分型检测试剂盒
Human Regulatory T Cell Staining Kit 人调节性T细胞染色试剂盒
- ¥2,970.00 – ¥9,370.00
-


- KTR201 27 Citations
- Th/Treg分型检测试剂盒
Mouse Regulatory T Cell Staining Kit小鼠调节性T细胞染色试剂盒
- ¥1,490.00 – ¥4,570.00
-


- IC001 15 Citations
- 固定破膜剂
FoxP3/Transcription Factor Staining Buffer Kit
- ¥320.00 – ¥1,140.00
试剂盒组分(以小鼠Th1/Th2检测为例)

样本采集及制备
血液样本
小鼠血液样本一般采用眼眶后静脉丛采血法,因此法不需麻醉或处死小鼠,对小鼠的伤害小,且可重复采血,具体方法如下:
- 穿刺采用一根特制的长7~10 cm硬的玻璃取血管,其一端内径为1~1.5 mm,另一端逐渐扩大,细端长约1cm即可,将取血管浸入1%肝素溶液,干燥后使用;
- 采血时,左手拇指及食指抓住鼠两耳之间的皮肤使鼠固定,并轻轻压迫颈部两侧,阻碍静脉回流,使眼球充分外突;
- 右手持取血管,将其尖端插入内眼角与眼球之间,轻轻向眼底方向刺入,当感到有阻力时即停止刺入,旋转取血管以切开静脉丛,血液即流入取血管中;
- 采血结束后,拔出取血管,放松左手,出血即停止。
注:
- 用本法在短期内可重复采血。小鼠一次可采血 0.2~0.3 ml;
- 为适用于Th1/Th2检测,需用肝素钠来处理取血管,不可用肝素锂、EDTA或枸橼酸钠。
脾单细胞悬液的制备
脾单细胞悬液的制备通常有两种方法,可依据自己的喜好及习惯来选择。
研磨法
- 小鼠用CO2处死,立即无菌取脾;
- 将脾浸入装有冷PBS的培养皿中,用钝头剪刀剪去白色的结缔组织,换入另一个装有冷 PBS的培养皿中以清洗脾脏;
- 再次换入一个装有冷PBS的培养皿中;
- 用小的弯头手术剪剪切脾脏成3 mm 左右的小块;
- 用5 mL或10 ml塑料一次性注射器的尾部背面轻轻按压研磨脾脏小块,此时会看到很多脾单细胞进入PBS中。对于一只30克左右的小鼠,完全研磨脾脏后约可获得100 x 106 左右的细胞;
- 经200目筛网过滤获得单细胞悬液,用冷PBS洗涤2次,每次1000 r/min, 离心10分钟;
- 将细胞悬浮于RPMI1640(含10%热灭活FBS)中,用台酚兰染色计数活细胞数(应在95%以上);
- 调节细胞浓度为2 x 106 /mL。
穿刺法
- 小鼠用CO2处死,立即无菌取脾;
- 将脾浸入装有冷PBS的培养皿中,用钝头剪刀剪去白色的结缔组织,换入另一个装有冷 PBS的培养皿中以清洗脾脏;
- 用10 mL注射器的针头在脾脏表面密密麻麻穿刺;
- 用针头吸取培养皿中的PBS,用力注入脾脏中,细胞即会从小孔中流出;
- 彻底冲出脾细胞,用玻璃吸管吸取细胞悬液;
- 经200目筛网过滤获得单细胞悬液,用冷PBS洗涤2次,每次1000 r/min, 离心10分钟;
- 将细胞悬浮于RPMI1640(含 10%热灭活FBS)中,用台酚兰染色计数活细胞数(应在95%以上);
- 调节细胞浓度为 2 x 106/mL。
淋巴结单细胞悬液的制备
- 小鼠用 CO2 处死,立即无菌取出腋下和腹股沟淋巴结;
- 将淋巴结浸入装有冷PBS的培养皿中,用钝头剪刀剪去脂肪组织,换入另一个装有冷PBS的培养皿中以清洗脾脏;
- 再次换入一个装有冷PBS的培养皿中;
- 用小的手术剪剪切淋巴结成3-4 mm大小的小块;
- 在培养皿中放置一个孔径为20 um的筛网,用5 ml或10 ml塑料一次性注射器的尾部背面轻轻按压小块,使得淋巴结的单细胞通过筛网进入其下面的PBS液中;
- 用冷PBS洗涤2次,每次1000 r/min, 离心10分钟;
- 将细胞悬浮于 RPMI 1640(含 10%热灭活FBS)中,用台酚兰染色计数活细胞数(应在95%以上);
- 调节细胞浓度为 2 x 106/ml。
刺激及染色
-
- 对于肝素抗凝血,取125 μl抗凝血至流式管中,加入125 μl不含血清的培养基和1μl PMA/Ionomycin Mixture (250×)和1 μl BFA/Monensin Mixture (250×)。取125 μl抗凝血和125 μl不含血清的培养基,作为对照。混匀,37℃孵育4-6小时,每隔1-2小时取出震荡混匀;
注:肝素抗凝血样本也可选择方法1b进行处理,在我们的试验结果中,比全血样本能检测到更多的细胞因子,原因未知; - 对于使用其它抗凝剂(如EDTA、枸橼酸钠)抗凝血,用淋巴细胞分离液分离外周血单个核细胞 (PBMCs)。用含10%胎牛血清的培养基重悬沉淀,使细胞浓度为1×107/ml。取250μl PBMCs至流式管中,加入1 μl PMA/Ionomycin Mixture (250×) 和1 μl BFA/Monensin Mixture (250×)。以只含PBMCs的样本作为对照。混匀,37℃孵育4-6小时,每隔1-2小时取出震荡混匀;
- 对于脾脏组织,使用适当的方法制备成单细胞悬液,并去除团块。(可选)使用淋巴细胞分离液分离制备脾单个核细胞。用含10%胎牛血清的培养基重悬沉淀,使细胞浓度为1×107/ml。取250 μl细胞悬液至流式管中,加入1 μl PMA/Ionomycin Mixture (250×)和1 μl BFA/Monensin Mixture (250×)。以只含细胞悬液的样本作为对照。混匀,37℃孵育4-6小时,每隔1-2小时取出震荡混匀;
注:在我们的试验结果中,脾细胞经淋巴细胞分离液分离后能检测到更多的细胞因子,原因未知;
- 对于肝素抗凝血,取125 μl抗凝血至流式管中,加入125 μl不含血清的培养基和1μl PMA/Ionomycin Mixture (250×)和1 μl BFA/Monensin Mixture (250×)。取125 μl抗凝血和125 μl不含血清的培养基,作为对照。混匀,37℃孵育4-6小时,每隔1-2小时取出震荡混匀;
- 从样本管和对照管中取100 μl细胞悬液至新的流式管中,加入5 μl Anti-Mouse CD3ε, FITC 和5 μl Anti-Mouse CD4, PerCP-Cy5.5。震荡混匀,室温避光孵育15分钟;
- 每管加入100 μl FIX & PERM Medium A,震荡混匀,室温避光孵育15分钟;
- 用蒸馏水将10× Flow Cytometry Staining Buffer稀释为1×,每管加入2 ml预冷1×Flow Cytometry Staining Buffer,300 g离心5分钟,弃上清;
注:液体尽量倒干净,不要有残留; - 每管加入100 μl FIX & PERM Medium B、5 μl Anti-Mouse IFN-γ, PE和5 μl Anti-Mouse IL-4, APC。震荡混匀,室温避光孵育15分钟;
- 每管加入 2 ml 1× Flow Cytometry Staining Buffer,300 g离心5分钟,弃上清;
- 每管加入500 μl 1× Flow Cytometry Staining Buffer重悬,上机检测;或者加入500 μl 1-4%多聚甲醛重悬,2-8℃避光,于24小时内检测。
流式检测
1 调节电压和补偿
推荐使用补偿微球对流式细胞仪进行电压和补偿调节。补偿微球通常比目的细胞小,在调节FSC/SSC电压和细胞设门时需要注意。
2 正确设门以得到Th1和Th2细胞在CD3+ CD4+辅助T细胞中的比例
注:至少获取20000-30000 CD3+ CD4+ T细胞。对于某一细胞因子,因品系和个体差异,分泌该细胞因子的细胞比例差异很大。为了进行统计学差异比较,请获取足够多的细胞样本。需要注意的是,PMA/Ionomycin刺激的细胞中,分泌IL-4的细胞非常低,甚至可忽略。此时,可考虑IL-4的极化培养。
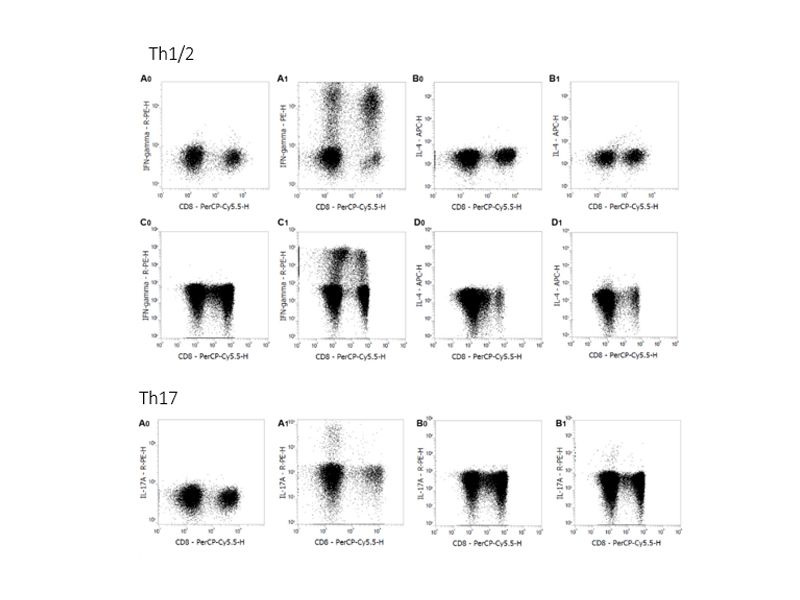
结果示例


使用Mouse Th1/Th2 Staining Kit进行流式检测。正常ICR小鼠的静息肝素抗凝血(A0, B0)、EDTA抗凝血来源的PBMCs (C0, D0)、脾细胞(E0, F0)和脾单个核细胞(G0, H0)染色IFN-γ和IL-4。正常ICR小鼠的 PMA/Ionomycin刺激的肝素抗凝血(A1, B1)、EDTA抗凝血来源的PBMCs (C1, D1)、脾细胞(E1, F1)和脾单个核细胞(G1, H1)染色IFN-γ和IL-4。对CD3+/CD4+细胞进行设门分析。