文章目录[隐藏]
传统的癌症治疗方法——化疗及肿瘤切除,分别面临着多重耐药和复发的问题。因此,肿瘤免疫治疗应运而生。免疫治疗通过激活机体的整个免疫系统来攻击肿瘤细胞以达到治疗目的。
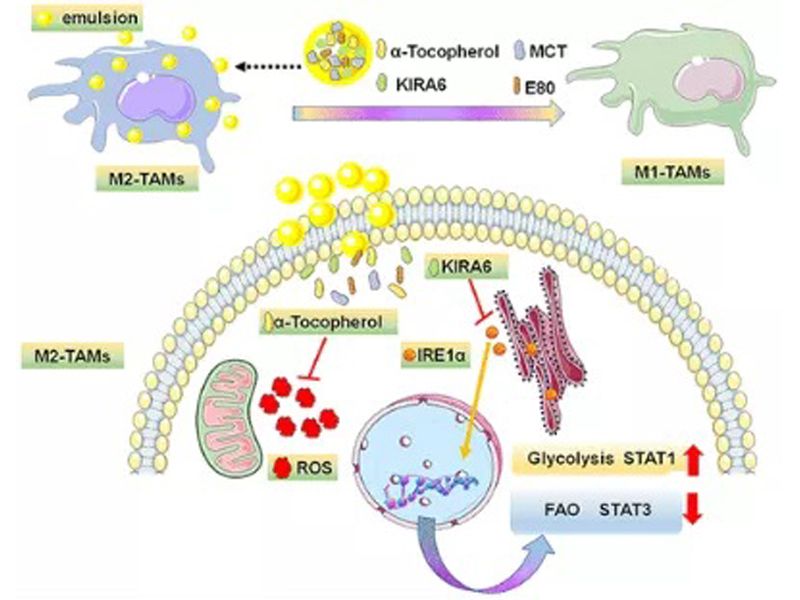
肿瘤相关巨噬细胞(tumor-associated macrophages, TAMs)是肿瘤中最重要的免疫抑制细胞,与肿瘤的扩散转移密切相关。巨噬细胞可分为具有抗肿瘤作用的M1型和促进肿瘤生长的M2型,且二者的表型可以在一定的刺激条件下转化。M2巨噬细胞转化(极化)为M1巨噬细胞可增强TNF-α、IL-6的分泌,激活抗肿瘤免疫应答,重塑免疫抑制肿瘤微环境,杀死肿瘤细胞。许多报道已经证明,基于这种“化敌为友”策略的药物输送系统可以有效地治疗肿瘤。
免疫原性细胞死亡(immunogenic cell death, ICD)是激活抗肿瘤免疫的另一种手段,以增强抗肿瘤免疫应答,提高肿瘤治疗效率。
细菌治疗是一种新型的肿瘤治疗方法,既可独立使用,也可与传统治疗方法结合使用。细菌可以抑制肿瘤血管的生成,激活机体免疫,从而抑制肿瘤的生长和转移。而且,细菌能够诱导不同模式的巨噬细胞极化。肿瘤的缺氧坏死带可以为厌氧菌和兼性厌氧菌提供靶向目标和缺氧条件,这对它们在肿瘤中的定殖是必要的。由于具有靶向肿瘤的能力,细菌也可以“装载”治疗药物,将其准确地递送至肿瘤部位。
但是, TAM极化、免疫原性细胞死亡(ICD)和细菌疗法又都有自身的局限性。作为一种应对措施,将它们结合用于治疗可提高抗肿瘤效果。
西南交通大学的研究团队在《Nano Letters》上发表了题为Polarization of Tumor-Associated Macrophages by Nanoparticle-Loaded Escherichia coli Combined with Immunogenic Cell Death for Cancer Immunotherapy(IF:11.189)的文章。

文章介绍了他们开发的一种装载纳米颗粒的大肠细菌系统Ec-PR848,该系统可用于靶向肿瘤的药物递送和巨噬细胞极化。当该系统与诱导ICD的PDOX结合使用时,可以增强巨噬细胞极化效应,增强T淋巴细胞在肿瘤组织中的浸润,激活抗肿瘤免疫反应,抑制肿瘤生长。该研究为提高肿瘤免疫治疗效率提供了一种新的策略。
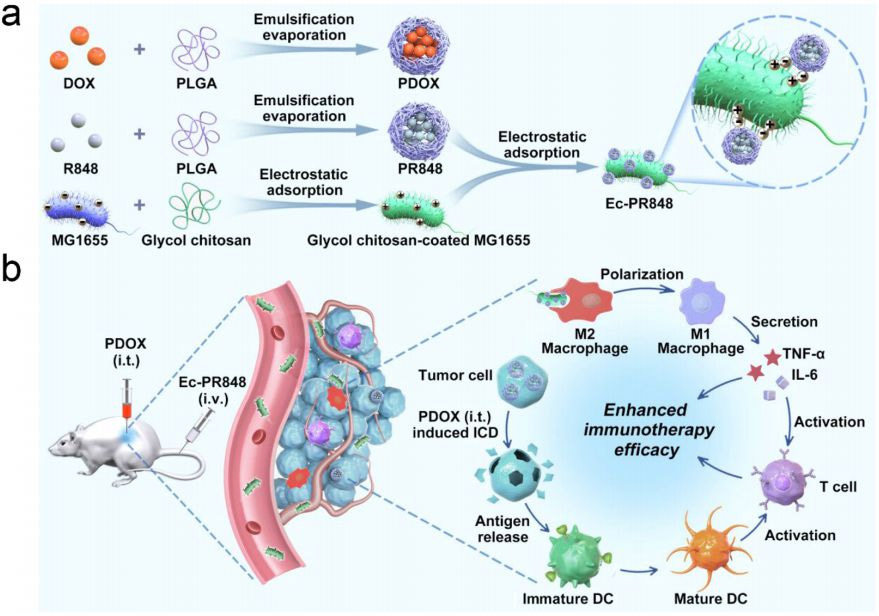
(b) 免疫原性细胞死亡(ICD)增强基于肿瘤相关巨噬细胞极化的免疫治疗效果
研究结果
1 体外诱导 ICD
为了证明制备的PDOX系统可以诱导ICD,研究团队以CRT(ICD的标志之一)为检测指标,在体外进行了验证。结果表明,PDOX能有效在体外触发ICD。
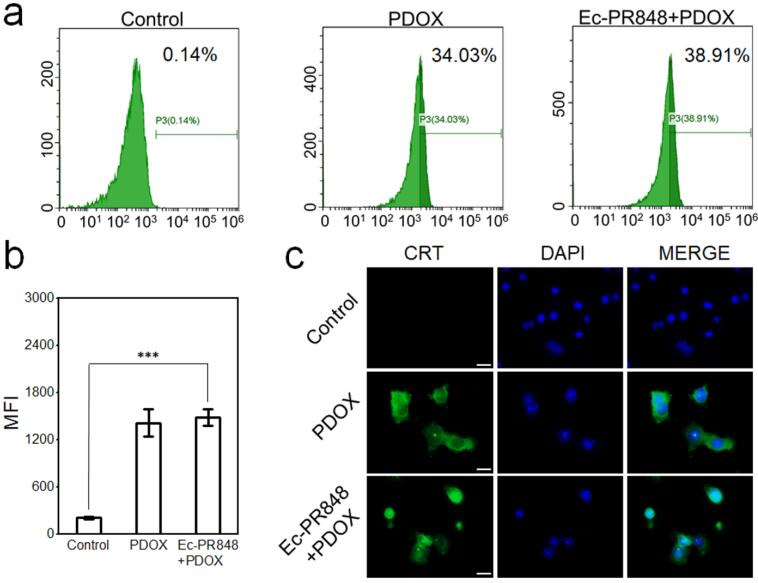
2 巨噬细胞体外极化
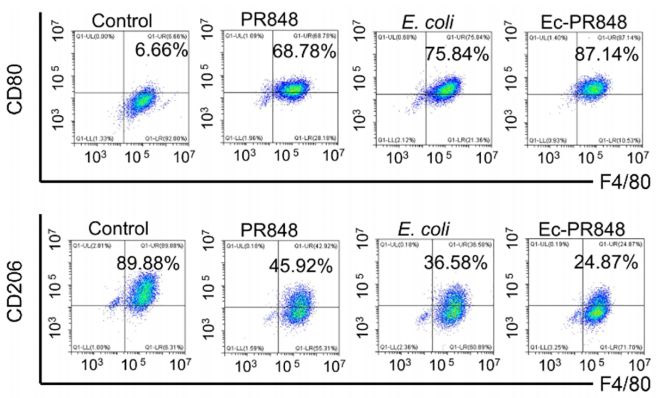
Resiquimod (R848)作为一种免疫调节药,能够激活相关通路使M2巨噬细胞极化为M1巨噬细胞。为了研究R848和大肠杆菌对巨噬细胞极化的影响,研究团队设置了空白对照、PR848、E.coli、Ec-PR848(PR848与E.coli结合)四个组别,分别对小鼠M2巨噬细胞进行诱导极化。
FCM分析结果显示,与对照组相比,PR848、E.coli和Ec-PR848能显著减少M2巨噬细胞数量(F4/80+ CD206+),增加M1巨噬细胞数量(F4/80+ CD80+);在这三种组别中,Ec-PR848组M1表型阳性率最高,M2表型阳性率最低。该结果表明三者都能够有效诱导M2巨噬细胞向M1巨噬细胞极化,且PR848与E.coli结合使用(Ec-PR848)可协同作用,更高效地促进M2巨噬细胞转化为M1巨噬细胞。
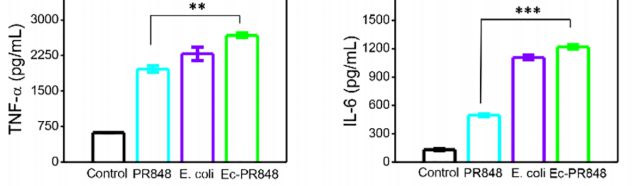
与此同时,研究团队利用ELISA试剂盒检测了M1巨噬细胞分泌的TNF-α和IL-6细胞因子。结果显示,PR848、E.coli和Ec-PR848均可明显增强TNF-α和IL-6的分泌;相较于对照组,PR848与E.coli的结合使用使得TNF-α和IL-6分泌量分别增加了3.28倍和2.32倍。
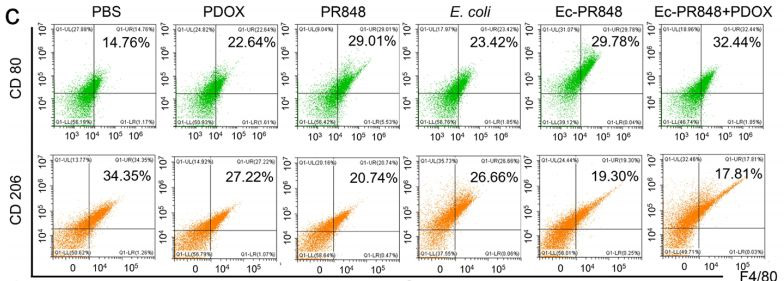
3 体内抗肿瘤免疫的激活
研究人员首先将乳腺癌4T1肿瘤细胞注射至小鼠体内以构建原位乳腺癌模型,之后分别将PDOX、PR848、E.coli、Ec-PR848以及Ec-PR848+PDOX5静脉注射至小鼠体内以诱导M2巨噬细胞向M1巨噬细胞极化。FCM分析结果表明, Ec-PR848能够有效地在体内诱导M2巨噬细胞极化,且值得注意的是,PDOX可进一步促进M2巨噬细胞的极化。
4 体内抗肿瘤作用
研究团队利用4T1乳腺癌模型小鼠进行了治疗性研究,以评估多种配方的抗肿瘤效果。研究结果显示,PDOX、E.coli、PR848以及Ec-PR848均具有不同程度的抗肿瘤效果,但效果并不显著。Ec-PR848与PDOX结合使用则具有显著的抗肿瘤效果,该组小鼠体内的肿瘤平均体积仅有192.78 mm3,比PBS组小鼠体内的肿瘤平均体积缩小12倍之多。
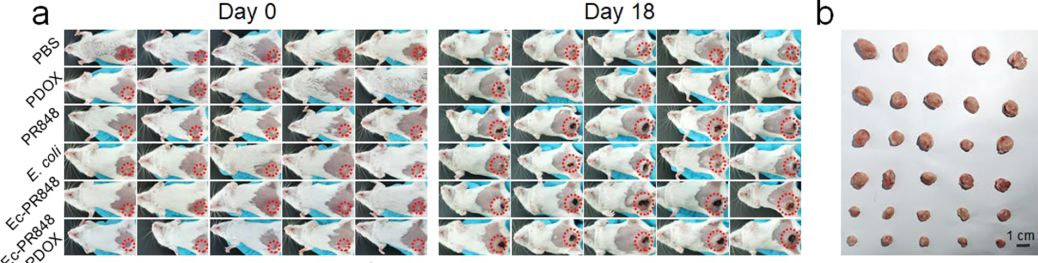
该研究证实了装载药物的E.coli系统可用于靶向肿瘤的药物递送和巨噬细胞极化,且当该系统与PDOX结合使用时,可以增强巨噬细胞极化效应和抗肿瘤免疫反应,为提高肿瘤免疫治疗的效率提供了一种新的策略。
MULTISCIENCES / 联科生物助力科研
在本研究中,研究人员使用了联科自主研发的ELISA试剂盒检测小鼠TNF-α和IL-6细胞因子,获得了很好的实验结果。联科生物衷心地祝贺该团队取得了优秀的研究成果!

联科生物从事ELISA试剂盒研发多年,已推出近460多种产品,包含普通和高敏两个系列,质控严格,满足您的多种需求。了解更多信息,请联系客服4006721600~