CCL2是最著名的CC趋化因子。CCL2对单核细胞和嗜碱性粒细胞具有趋化活性。它是调节单核细胞/巨噬细胞迁移和浸润的关键趋化因子之一。在如下诸多疾病中发挥作用。
1 癌 症
CCL2在肿瘤发展进程中发挥作用。在许多癌症类型中,CCL2信号具有促肿瘤作用。在乳腺癌、结直肠癌、前列腺癌、黑色素瘤、胃癌和卵巢癌患者中,CCL2水平升高通常与疾病进展相关。CCL2的过度表达或基因变体的存在与巨噬细胞募集和患者预后不良有关。例如,CCL2信号转导被证明是结直肠癌发展的一个重要前驱物,CCL2-/-小鼠中CCL2信号的缺失阻碍了肿瘤的进展。在乳腺癌中,CCL2-CCR2信号转导是导致肺转移的重要初始事件;在前列腺癌中,除了促进癌细胞增殖和迁移外,CCL2通过激活PI3K/Akt/survivin通路保护前列腺癌细胞免于自噬死亡。此外,CCL2还介导前列腺肿瘤微环境中的基质细胞反应。在黑色素瘤和胰腺小鼠模型中,siRNA敲除CCL2或抗体中和抑制树突状细胞和树突状细胞的募集,并减少肿瘤生长和转移。阻断CCL2抑制肿瘤生长,减少CD68+巨噬细胞浸润,并导致肿瘤相关微血管减少。这些研究表明CCL2通过多种免疫细胞的募集和激活促进肿瘤的进展(图1)。不仅如此,CCL2-CCR2信号转导在肿瘤和间质细胞中具有其他多种关键功能(具体可参见Lim等人文章中所做的总结)(Lim, Yuzhalin et al. 2016)。CCL2通过抑制细胞凋亡、坏死和自噬等过程提高癌细胞的存活。
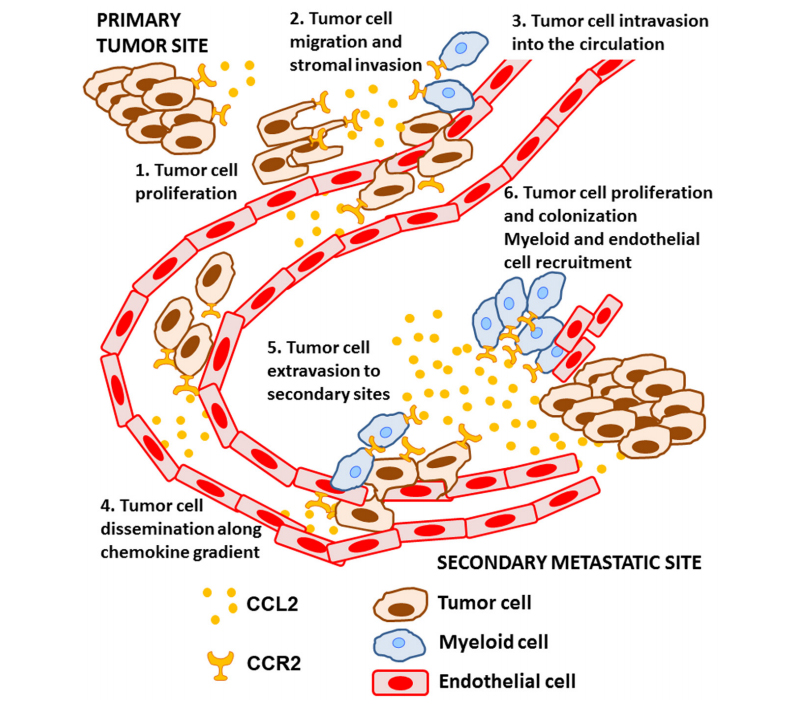 |
| 图1. CCL2-CCR2信号在癌细胞转移过程中的作用 |
然而,在卵巢癌、胰腺癌和非小细胞肺癌中,CCL2蛋白表达和巨噬细胞募集与良好的生存率相关。CCL2在结肠癌细胞或大鼠胶质肉瘤细胞中的过度表达抑制小鼠的肿瘤发展,并与注射部位M1巨噬细胞的募集有关。在某些HCC动物模型中,CCL2也与M1巨噬细胞募集有关。在B16黑色素瘤模型中,CCL2/CCR2信号介导γδT细胞的募集,γδT细胞表达IFN-γ,对癌细胞具有细胞毒性。在乳腺癌中,一项研究表明,中性粒细胞在原发性肿瘤中被CCL2激活,并对肺转移细胞产生细胞毒性,从而抑制了肿瘤生长。
这些研究表明,CCL2通过以环境和组织依赖的方式招募免疫细胞来参与肿瘤的进程。
2 骨 重 塑 与 骨 转 移
CCL2调节生理性骨重建,以响应激素和机械刺激。由其驱动的骨疾病和骨相关癌症之间存在潜在的病理关系。在骨重塑和骨相关肿瘤中的作用使其成为一种新的抗吸收和抗转移靶点。
研究表明,CCL2促进破骨细胞前体细胞的迁移,促进破骨细胞的发生和骨吸收。CCL2和CCR2基因变异是骨质疏松症的危险因素。CCL2在骨质疏松性骨和前列腺癌引起的骨吸收中有广泛表达。成骨细胞CCL2的时空表达与炎症过程中单核细胞的募集和发育调控骨重建有关。外源性CCL2可增强炎症骨中单核细胞的募集。CCR2基因缺失小鼠的骨量较高,破骨细胞数量、大小和活性降低。
甲状旁腺激素(PTH)对骨骼有多方面的影响。CCL2对甲状旁腺素的合成代谢和分解代谢作用都是必不可少的。成骨细胞通过将甲状旁腺激素(PTH)与其受体甲状旁腺激素/甲状旁腺激素相关肽受体(PTH1R)结合而分泌CCL2。甲状旁腺素诱导的CCL2促进单核细胞和骨前体募集到重塑位点。同时,CCL2还参与了成骨细胞向成熟破骨细胞的融合。CCL2表达的短暂增加以及由此产生的破骨细胞活性是PTH对骨的合成代谢作用所必需的。肿瘤细胞产生甲状旁腺激素相关肽(PTHrP),刺激成骨细胞CCL2的表达。成骨细胞CCL2增加破骨细胞生成和骨吸收,促进骨肿瘤生长(图2)(Siddiqui and Partridge 2017)。
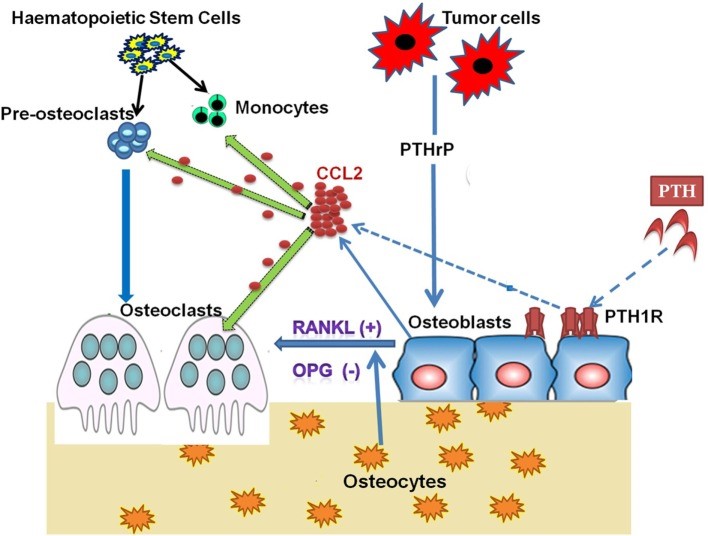 |
| 图2. CCL2参与PTH/PTHrP对骨细胞的作用 |
与PTH相关蛋白(PTHrP)协同作用,CCL2介导肿瘤源性因子与宿主源性趋化因子的相互作用,促进骨转移。在乳腺癌和前列腺癌中,溶骨性级联反应由肿瘤细胞源性PTHrP驱动,PTHrP上调成骨细胞中的CCL2/MCP-1。PTHrP与成骨细胞CCL2表达之间的这种关系可能会促使浸润性乳腺癌细胞在骨中的定居。
3 自 身 免 疫 性 疾 病
大多数自身免疫性疾病的特点是淋巴髓细胞浸润到靶组织,导致炎症和组织损伤。这个过程是由趋化因子在一个复杂的免疫细胞网络中充当信号桥梁。许多研究已经阐明了单核细胞在不同的自身免疫性疾病中募集的分子基础,其结论指出单核细胞趋化蛋白1(MCP-1),也即CCL2及其细胞表面受体CCR2起主要作用。这些发现表明,通过干扰CCL2或其受体,有可能抑制CCR2依赖性疾病的进展。
患有银屑病和其他皮肤疾病的住院患者中CCL2的表达升高[20,21]。研究表明,CCL2由PSO患者皮肤角质形成细胞产生,并通过肿瘤坏死因子α(TNF-α)和干扰素-γ(IFN-γ)协同放大。角质形成细胞释放CCL2后,单核细胞通过CCR2发出化学触觉信号,并从血液循环迁移到皮肤,在那里它们分化为巨噬细胞,巨噬细胞能够作为抗原提呈细胞并分泌TNF-α(图3)。
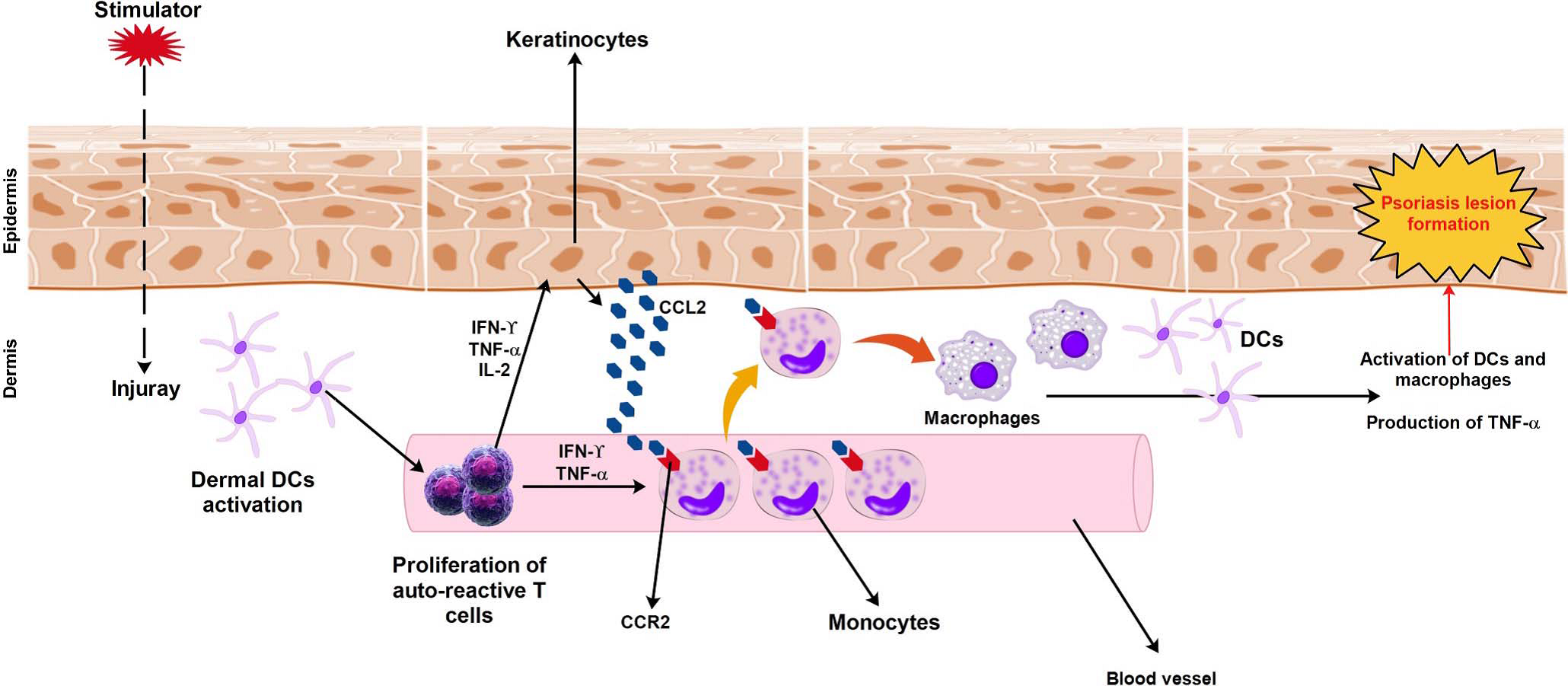 |
| 图3.不同细胞类型参与银屑病皮损的形成。 |
CCL2/MCP1是系统性红斑狼疮和狼疮性肾炎的新靶点。在狼疮性肾炎中,CCL2/MCP-1及其趋化因子受体CCR2备受关注,因为CCL2/CCR2介导了巨噬细胞和T细胞在肾炎肾脏中的募集。狼疮性肾炎在CCL2或CCR2缺陷的自身免疫小鼠中明显减轻。针对CCL2基因突变的流行病学研究支持CCL2介导肾脏炎症的假说。同时,实验研究表明,几种CCL2拮抗剂可以控制已建立的狼疮性肾炎。
CCL2被认为在硬皮病中也起重要作用。
4 神 经 系 统 疾 病
CCL2及其受体CCR2已被证明在急性脑外伤,如中风,以及各种神经退行性疾病,包括阿尔茨海默病、多发性硬化症和缺血性脑损伤中发挥作用 (Conductier, Blondeau et al. 2010)。
多发性硬化(MS)是人类中枢神经系统(CNS)最常见的炎症性脱髓鞘疾病。实验性自身免疫性脑脊髓炎(EAE)的描述、转基因、敲除和中和研究的证据表明,CCL2和CCR2在炎症性浸润进入中枢神经系统中起非冗余作用。因此,CCL2和CCR2可能是MS特异有效治疗的靶点。
缺氧缺血性脑损伤(HIBD)是一种常见的脑损伤类型,它是由损伤引起的大脑皮质浅层出血,软脑膜完整。CCR2广泛分布于脑神经元、星形胶质细胞和小胶质细胞中,是脑组织中主要的趋化因子受体。作为CCR2的配体,CCL2在炎症反应中起重要作用。参与HIBD病程。
神经源性疼痛对周围神经损伤的反应很大程度上依赖于位于脊髓背角的小胶质细胞。近年来,CCL2和CCL21被认为是介导受损神经元与小胶质细胞通讯的潜在因素。
CCL2/CCR2在促进巨噬细胞和中性粒细胞浸润到局灶性脑损伤后的实质中发挥作用。
CCL2在肌萎缩侧索硬化症中表达上升,尤其是,CCL2和CXCL-8水平与ALS功能评定量表(ALSFRS-R)呈负相关。
在急性脑外伤,如中风,以及慢性病如多发性硬化症或阿尔茨海默病时,炎症发生以“清理”病变并限制其面积。然而,长期持续的炎症可能有细胞毒性作用,加重发病率和疾病的严重程度。在与神经元死亡相关的炎症反应中,CCL2及其受体CCR2尤为重要。
获得性免疫缺陷综合征(AIDS)脑病是人类免疫缺陷病毒(HIV)或猿猴免疫缺陷病毒(SIV)感染者的一种严重而频繁的并发症。HIV和SIV-Nef蛋白是艾滋病病理学中的一个进展因子,它诱导CCL2的表达,进而促进HIV和SIV的神经毒力。所以CCL2用于辅助靶向治疗HIV感染者。
5 细 菌 与 病 毒 感 染
在HIV感染者中发现高水平的CCL2/CCR2。CCL2/CCR2轴与高水平的免疫激活和炎症密切相关,这是HIV感染的标志,即使在接受抗逆转录病毒治疗的患者中也是如此。此外,CCL2增加HIV的复制。CCL2/CCR2驱动效应的调节可能对HIV疾病的进展产生重大影响。CCL2可能是治疗HIV-1感染的抗炎靶点。
另外,CCL2的高表达与严重急性呼吸综合征冠状病毒2(SARS-CoV-2)感染有关
6 其 他
除上面所述疾病外,CCL2还参与其他多种疾病过程的发病机制,包括血管通透性和转移过程中免疫细胞的吸引、肝炎、高血压、高血脂、糖尿病、冠心病等。
CCL2与肝脏炎症之间有着显著的关系。酒精性肝炎患者炎症部位的肝实质细胞中CCL2的表达增强,外周静脉和肝静脉中CCL2的浓度也增加,说明在刺激炎症浸润中起重要作用。
CCL2水平升高会增加高血压、高脂血症、2型糖尿病和冠心病的风险。用丙锗抑制CCR2受体,改善糖尿病小鼠的胰岛素抵抗和肝脂肪变性。CCL2是糖尿病肾病炎症、肾损伤和纤维化的主要促进剂。研究人员发现糖尿病可诱导肾脏MCP-1的产生,尿MCP-1水平可用于评估肾脏炎症。此外,在啮齿类动物中进行的基因缺失和分子阻断研究已经确定MCP-1是治疗糖尿病肾病的重要靶点。有证据还表明,人类MCP-1基因多态性与2型糖尿病进展性肾功能衰竭有关。
CCL2参与动脉粥样硬化斑块的形成、发展和失稳,并在梗死后重建中起重要作用。血浆MCP-1水平在急性冠脉综合征(ACS)急性期和慢性期具有预后价值。MCP-1轴可能是ACS患者治疗的一个有吸引力的靶点。阻断CCL2的表达可能是治疗动脉粥样硬化和冠心病的有效方法。
老年性黄斑变性(AMD)的病因尚不清楚。但CCL2似乎在AMD视网膜下小胶质细胞和巨噬细胞聚集中起重要作用,并参与视网膜变性和脉络膜新生血管的形成。
总之,CCL2是一个功能多样的基因。联科生物自主研发的大鼠CCL2也于9月份上市。联科生物在试剂盒研发和生产的每一个环节都进行严格的质控,值得您信赖!联科生物已有绝大多数趋化因子ELISA试剂盒欢迎选购!
| 目录号 |
产品名称 |
| EK187 |
Human CCL2/MCP-1 ELISA Kit |
| EK161 |
Human CCL3/MIP-1α ELISA Kit |
| EK162 |
Human CCL4/MIP-1β ELISA Kit |
| EK1129 |
Human CCL5/RANTES ELISA Kit |
| EK1130 |
Human CCL11/Eotaxin ELISA Kit |
| EK167 |
Human CCL13/MCP-4 ELISA Kit |
| EK1288 |
Human CCL16/HCC-4/NCC-4 ELISA Kit |
| EK1115 |
Human CCL17/TARC ELISA Kit |
| EK1148 |
Human CCL18/PARC ELISA Kit |
| EK1211 |
Human CCL20/MIP-3α ELISA Kit |
| EK1291 |
Human CCL25/TECK ELISA Kit |
| EK1150 |
Human CCL26/Eotaxin-3 ELISA Kit |
| EK1214 |
Human CCL27/CTACK ELISA Kit |
| EK196 |
Human CXCL1/KC ELISA Kit |
| EK1265 |
Human CXCL3/GRO-γ ELISA Kit |
| EK1219 |
Human CXCL5/ENA-78 ELISA Kit |
| EK1143 |
Human CXCL9/MIG ELISA Kit |
| EK168 |
Human CXCL10/IP-10 ELISA Kit |
| EK1207 |
Human CXCL11/I-TAC ELISA Kit |
| EK1119 |
Human CXCL12/SDF-1 ELISA Kit |
| EK1105 |
Human CXCL13/BLC/BCA-1 ELISA Kit |
| EK1254 |
Human CXCL16 ELISA Kit |
| EK1209 |
Human CX3CL1/Fractalkine ELISA Kit |
| EK287 |
Mouse CCL2/MCP-1 ELISA Kit |
| EK287HS |
Mouse CCL2/MCP-1 High Sensitivity ELISA Kit |
| EK261 |
Mouse CCL3/MIP-1α ELISA Kit |
| EK262 |
Mouse CCL4/MIP-1β ELISA Kit |
| EK2129 |
Mouse CCL5/RANTES ELISA Kit |
| EK2130 |
Mouse CCL11/Eotaxin ELISA Kit |
| EK2211 |
Mouse CCL20/MIP-3α ELISA Kit |
| EK2216 |
Mouse CCL22/MDC ELISA Kit |
| EK296 |
Mouse CXCL1/KC ELISA Kit |
| EK2142 |
Mouse CXCL2/MIP-2 ELISA Kit |
| EK2143 |
Mouse CXCL9/MIG ELISA Kit |
| EK268 |
Mouse CXCL10/IP-10 ELISA Kit |
| EK387 |
Rat CCL2/JE/MCP-1 ELISA Kit |
| EK361 |
Rat CCL3/MIP-1α ELISA Kit |
| EK3129 |
Rat CCL5/RANTES ELISA Kit |
| EK396 |
Rat CXCL1/KC ELISA Kit |
| EK3142 |
Rat CXCL2/CINC-3 ELISA Kit |
本文参考文献包括但不限于:
• Conductier, G., N. Blondeau, A. Guyon, J. L. Nahon and C. Rovere (2010). "The role of monocyte chemoattractant protein MCP1/CCL2 in neuroinflammatory diseases." J Neuroimmunol 224(1-2): 93-100.• Lim, S. Y., A. E. Yuzhalin, A. N. Gordon-Weeks and R. J. Muschel (2016). "Targeting the CCL2-CCR2 signaling axis in cancer metastasis." Oncotarget 7(19): 28697-28710.• Siddiqui, J. A. and N. C. Partridge (2017). "CCL2/Monocyte Chemoattractant Protein 1 and Parathyroid Hormone Action on Bone." Front Endocrinol (Lausanne) 8: 49.
|