近日,中国科学院上海生命科学研究院生物化学与细胞生物学研究所胡荣贵研究组的最新研究成果,以Excessive UBE3A Dosage Impairs Retinoic Acid Signaling and Synaptic Plasticity in Autism Spectrum Disorders为题,在线发表在Cell Research上。该研究阐明了UBE3A过度激活抑制视黄酸(维甲酸)合成从而引起自闭症谱系障碍疾病(ASD)发生的分子机制,并发现潜在的治疗靶点。
自闭症谱系障碍,简称“自闭症”,又名“孤独症”,其核心症状表现为社会性交流和沟通的障碍,重复刻板行为,是严重的神经发育障碍性疾病。近年自闭症在世界范围内的发病率约为1.2%,且呈逐年急剧上升趋势。据统计,我国目前自闭症患者已超过1000万。二十世纪九十年代中期以来的研究表明,在自闭症病人中,染色体15q11-q13拷贝数扩增(CNV)的先证者占比1-3%;由此导致的泛素连接酶UBE3A基因的过表达是自闭症发生的重要因素之一。泛素连接酶UBE3A基因的缺失则与人类天使综合征(Angelman Syndrome)有关。UBE3A的生理功能及其突变引发疾病的机制一直是神经生物学研究的热点之一。
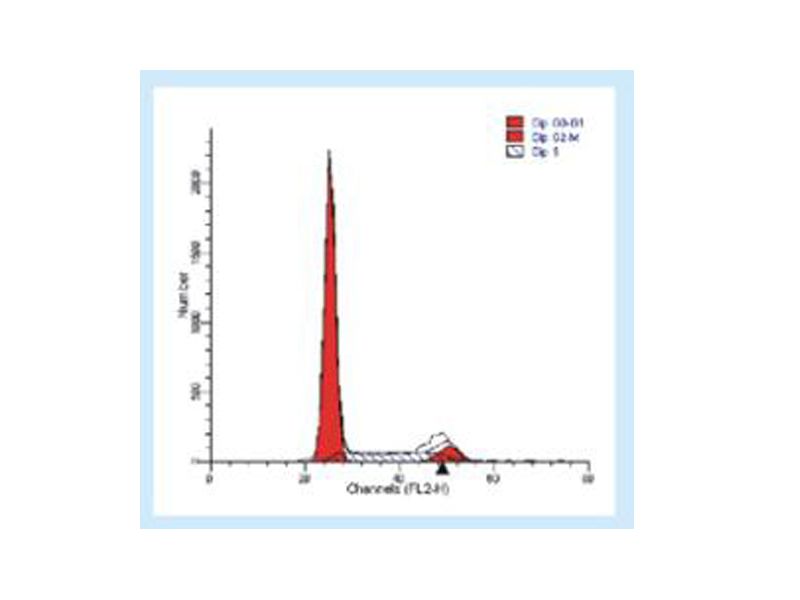
UBE3A(又名E6AP,因结合人乳头瘤病毒HPV编码的E6蛋白而得名) 是泛素研究领域最早被鉴定的泛素连接酶之一,根据其结构特征,定义一个涵盖大约40种蛋白的泛素连接酶HECT亚家族。从鉴定泛素连接酶UBE3A的酶学底物出发,研究首次发现UBE3A通过泛素化修饰视黄醛脱氢酶家族蛋白(维生素A代谢途径中,视黄醛转化成为视黄酸最重要的酶类)并抑制其视黄酸合成的催化活性。生化和电生理数据表明, UBE3A过表达导致神经元细胞中维甲酸水平的过度降低,以及破坏神经突触可塑性,并可能由此参与了自闭症的发生。在UBE3A过表达的小鼠自闭症模型中的实验表明,口服安全剂量的全反式维甲酸被发现能够显著缓解自闭症模型小鼠的一系列类似自闭症特征的行为,这为针对某些自闭症亚型的临床干预提供了非常有潜力的分子靶标和前期研究基础。
同时,研究发现ALDH1A的抑制剂(也是戒酒类药物Disulfiram,双硫仑)能够在小鼠中引发自闭症的特征行为,且能由口服维甲酸所缓解(未发表数据)。这一发现加强了“视黄酸合成抑制”与 自闭症行为之间的逻辑联系,也提醒人们目前在临床中被批准认为能安全使用的药物有可能存在增加胎儿或儿童罹患自闭症的风险。
该研究揭示了家族性人类自闭症谱系障碍的发病新机制,明确支持和进一步诠释了“人类自闭症既是一种神经系统发育缺陷也是一种神经系统运行性疾病”的理念;从全新的角度探讨了ASD发生的分子机制,为预防和治疗人类ASD带来新思路。
胡荣贵研究组长期从事蛋白质泛素信号领域的研究,近期工作包括发现泛素信号调节细胞自噬和建立一系列研究方法。研究中的自闭症患者的临床样本和遗传信息由中南大学教授夏昆、郭辉提供。研究工作得到了中科院分子细胞科学卓越创新中心、中科院战略先导计划、国家自然科学基金委医学部国家杰出青年基金、国家科技部重大专项、信号传导网络协同创新中心和中国博士后科学基金等的支持。该工作的数据收集得到了国家蛋白质科学中心·上海、生化与细胞所细胞生物学、分子生物学和动物实验技术平台的支持。
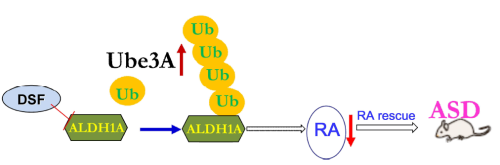
工作模型:泛素连接酶UBE3A的过度激活引发底物ALDH1A家族蛋白的过量泛素化,抑制视黄酸(RA)合成、破坏神经突触可塑性而导致自闭症(ASD)。