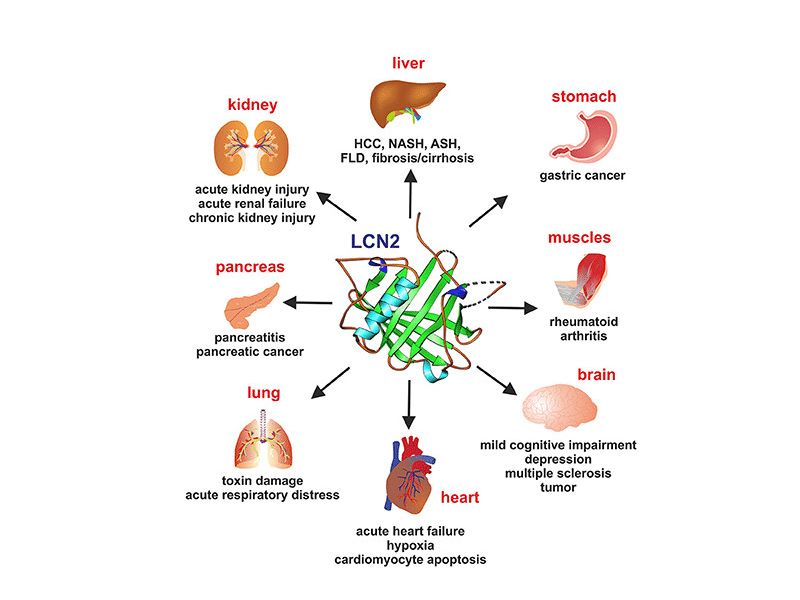
经甲醛固定的部分组织细胞,因固定过程中可能会形成醛键或羧甲基而封闭部分抗原决定簇,使免疫组化标记敏感性明显降低,因此在染色前,有些抗原需进行修复或暴露。
抗原修复方法可分为化学方法和物理方法。化学方法是以酶消化方法,常用胰蛋白酶及胃蛋白酶,配制浓度与消化时间要适度。常用的物理方法有单纯加热、微波处理和高压加热。在选用这三种方法时,浸泡切片的缓冲液的离子强度和pH、加热的温度和时间均影响着抗原修复效果。
1、pH的应用范围及选择
抗原修复液的pH非常重要,有效的抗原修复pH要比修复液的化学成分更重要,同样的修复液随着pH的升高染色的强度逐渐增强,但最佳pH范围为6.0-10.0。目前大家公认的最好的抗原修复液是pH6.0的柠檬酸盐缓冲液和pH8.0的EDTA缓冲液。作为通用修复液碱性pH的修复液要比酸性的有效,而对固定很长时间旧的存档组织,酸性pH的修复液则优于碱性的修复液。
2、抗原修复时应选择最佳温度
90℃的温度对未经固定的蛋白质可发生变性,但经福尔马林固定的蛋白质,温度必须达到92℃以上方能使其变性。研究结果显示,温度为92-98℃是合适的,95℃效果最好。
3、抗原修复液必须遵循自然降温规律,否则效果不好或达不到抗原修复的目的
抗原修复持续时间过后,取出放于室温中让其慢慢地降温,绝对不能为了争取时间,强行用冰块或冷水使其降温。这是因为当高温中的抗原蛋白分子链脱离了其他的束缚或联结,要有一个自然环境让其自然放松下来,随着温度的降低,它们会慢慢地恢复原来的形态和构型。
4、尽量使用足量的抗原修复液
应用于抗原修复的液体,一定要充足,防止切片干涸。应用大量的抗原修复液时,由于它的量较大,可延缓液体的沸腾时间,增加切片受微波辐射的量,对抗原修复将达到彻底。