文章目录[隐藏]
- 制备 PBMC,并调整细胞浓度至 107/mL。
- 在每个流式上样管中加入 100 μL 准备好的细胞悬液,细胞数约为 1 × 106 个。
- 按照细胞表面抗原染色方法标记 CD4 和 CD25。根据说明书和抗体管上的标识确定抗体用量(一般来说是 20μL,可能随批次有差异)。按个人要求设置空白管、对照管、补偿管和样本管。4℃ 孵育 30 分钟。
- 用预冷 PBS 溶液洗涤细胞,300-400 g 离心 5 分钟,去上清。
- 用 3 倍体积的固定/破膜稀释液 稀释 固定/破膜浓缩液,制成固定/破膜工作液,注意要新鲜配制,每个样本的用量为 1mL。
- 旋涡震荡重悬细胞后加入 1ml 的固定/破膜工作液(Fixation/Permeabilization)(1:3 稀释好),并再次旋涡混匀。
- 避光 4℃ 孵育 30 分钟到 60 分钟。
- 将破膜缓冲液用去离子水 1:9 稀释,制成工作液。每个样本的用量为 8.5mL。
- 无需洗涤,直接加入 2mL 破膜缓冲液工作液(Permeabilization Buffer)300-400 g 离心洗涤细胞并弃去上清液。
- (可选)重复第 9 步操作洗涤细胞。
- 加入 100 μL PBS 重悬细胞。
- (封闭可选)体系中加入 2% 的大鼠血清 2 μL,室温避光孵育 30 分钟。
- 体系加入适量的 Foxp3 抗体,对照管中加入适量的同型对照,具体用量参照说明书,避光 4℃孵育至少 30 分钟。建议进行预实验摸索出抗体的最适浓度。
- 加入 2mL 破膜缓冲液工作液离心洗涤细胞并弃去上清液。
- 重复上一步洗涤细胞。
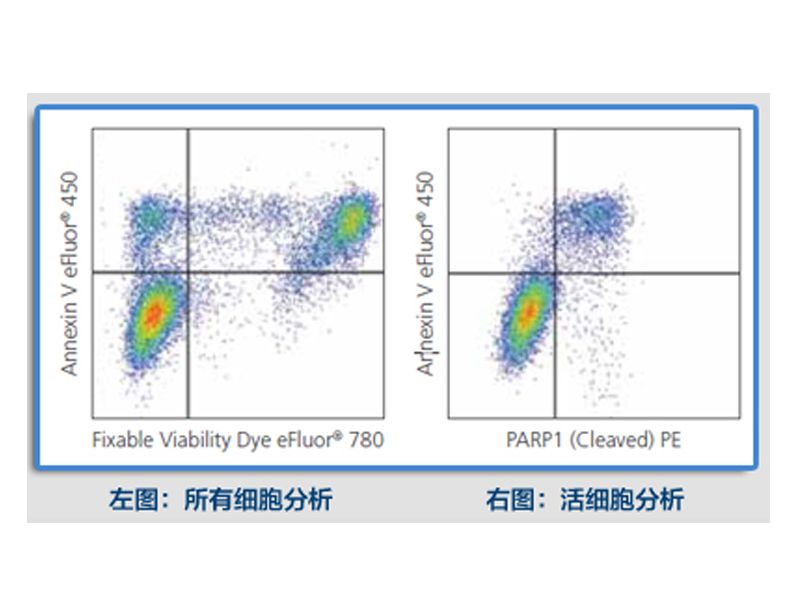
- 用适量体积的 Flow Cytometry Staining Buffer 重悬细胞,并上机检测并分析。注:由于染色过程中使用了细胞固定和破膜,对比起活细胞在形态上会有一定变化(一般是变小),因此 FSC/SSC 图中圈门时需要做一定调整。
注:以上说明书仅供参考,具体实验请对照附件厂商说明书操作。
联科生物Treg检测产品列表
-


- KTR101 4 Citations
- Th/Treg分型检测试剂盒
Human Regulatory T Cell Staining Kit 人调节性T细胞染色试剂盒
- ¥2,970.00 – ¥9,370.00
-


- KTR201 27 Citations
- Th/Treg分型检测试剂盒
Mouse Regulatory T Cell Staining Kit小鼠调节性T细胞染色试剂盒
- ¥1,490.00 – ¥4,570.00
-


- IC001 15 Citations
- 固定破膜剂
FoxP3/Transcription Factor Staining Buffer Kit
- ¥320.00 – ¥1,140.00