胶质母细胞瘤(GBM)是一种致命的原发性脑癌,在过去的十年中,免疫检查点阻断(ICBs)彻底改变了癌症治疗,但它们对GBM的临床疗效甚微。研究发现,在ICBs耐受的GBM患者中,PTEN基因突变显著富集。PTEN缺陷会激活磷脂酰肌醇3 - 激酶(PI3K)-AKT通路,形成免疫抑制微环境。因此,在PTEN缺陷的GBM患者中,克服ICBs的耐药性仍然是一个临床挑战。近年,溶瘤病毒(OV)在癌症治疗中被认为是有潜力的。PTEN缺陷的GBM有可能成为OV治疗的一个有希望的靶点。

最近,来自中山大学的研究团队在期刊Signal Transduction and targeted therapy上发表了题为Modulating the tumor microenvironment via oncolytic virus and PI3K inhibition synergistically restores immune checkpoint therapy response in PTEN-deficient glioblastoma的文章,介绍了一种化学-生物-免疫三联疗法来克服PTEN缺陷GBM的免疫耐药。
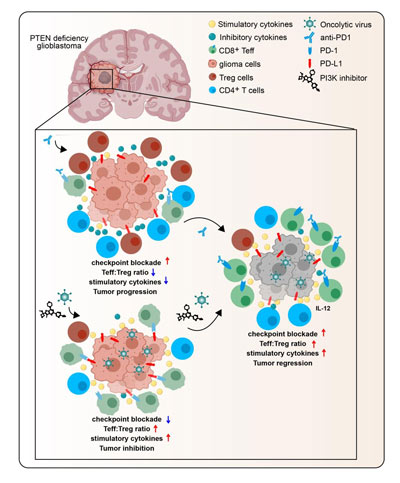
OV、PI3K抑制剂、ICB的联合治疗对肿瘤微环境的调节的示意图
该团队首先使用shRNA建立了PTEN敲除细胞系GL261,并在C57小鼠体内构建了原位异种移植模型。之后,研究团队发现, OV、PD-1阻断剂、PI3K抑制剂的三联疗法,能够诱导小鼠的肿瘤消退和提高小鼠生存率。此外,三联疗法增加了CD8+效应T细胞(Teffs)的比例,降低了调节性T细胞(Tregs)的数量,也显著增加了干扰素-γ和颗粒酶- B阳性CD8+ T细胞。长期存活的小鼠在第80天再次接受胶质瘤细胞增加2倍的挑战。大多数接受挑战的小鼠没有死于新的肿瘤,而所有年龄匹配的对照组小鼠在第20天死于肿瘤。上述结果表明了OV、PI3K抑制剂、PD-1阻断剂联合治疗的疗效显著,并能够在PTEN缺陷的GBM小鼠模型中建立长期的抗肿瘤免疫。
另外,OV配合PI3K抑制剂通过增强IL-12的分泌,重塑胶质瘤衍生的细胞因子表达模式,激活T细胞功能,重塑免疫抑制状态,介导抗肿瘤作用和肿瘤消退。
总之,该研究确定了PTEN缺陷是OV治疗的生物标志物,并表明靶向肿瘤来源的细胞因子是调节肿瘤微环境的一个有吸引力的策略,对GBM治疗有重要意义。
MULTISCIENCES产品支撑:
Annexin V-APC/PI apoptosis kit (AP107)