文章目录[隐藏]
本文主要讲述了谷氨酰胺代谢微环境驱动M2巨噬细胞极化,介导人表皮生长因子受体-2(HER2)阳性胃癌曲妥珠单抗耐药的研究。研究人员发现,谷氨酰胺代谢关键酶GLS在曲妥珠单抗治疗失败的病人中表达升高, 而GLS通过驱动M2型巨噬细胞极化,促进肿瘤相关成纤维细胞转化和CCL2/CCR2炎症轴激活,从而介导肿瘤细胞对曲妥珠单抗的抵抗。
胃癌是世界范围内最常见的恶性肿瘤之一。在中国,超过70%的患者被诊断为晚期,其中大约20%的进展期胃癌患者均为HER2阳性。该类患者一般预后不佳,复发率高。
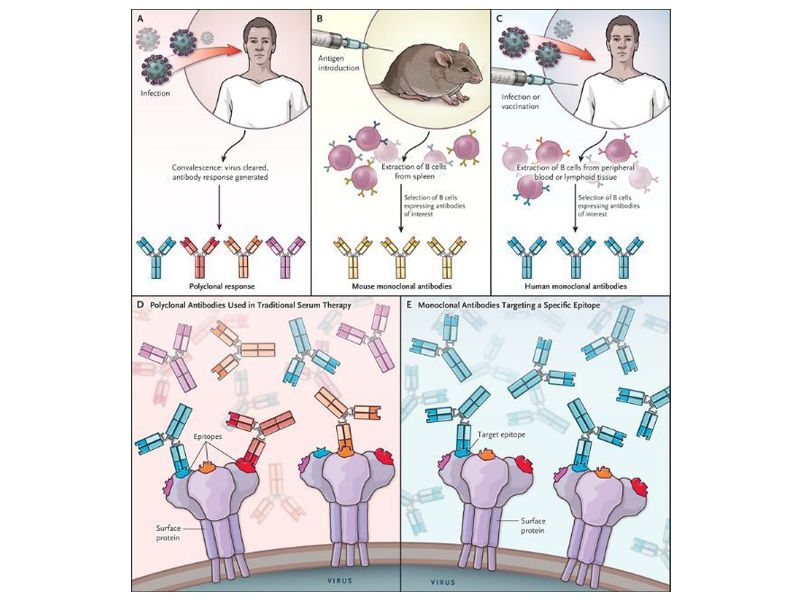
曲妥珠单抗是一种针对HER2的人源化单抗。曲妥珠单抗用于胃癌的研究发现,曲妥珠单抗联合化疗可以显著提高HER2阳性胃癌患者的生存率,从而确立了曲妥珠单抗作为HER2阳性胃癌的一线靶向疗法的地位,然而,大多数患者在曲妥珠单抗持续治疗后的一年内会产生获得性耐药性,使其治疗效果受到了强烈的抑制阻碍,目前仍无有效的逆转措施。
目前科研上对曲妥珠单抗耐药机制的研究主要集中在肿瘤细胞本身的内在特征,如旁路通路胰岛素样生长因子1受体、HER3等的激活和下游信号通路的上调。而肿瘤细胞除了自身固有的特性外,还存在于复杂的微环境中,现如今对环境介导的耐药机制了解甚少,微环境中的代谢过程不断地、动态地变化,使得不同免疫细胞亚群的分化,导致整个微环境朝着促进肿瘤的方向发展。
巨噬细胞,包括促炎症的M1和抗炎的M2巨噬细胞,是肿瘤微环境的重要组成部分。M1和M2巨噬细胞的代谢存在显著差异。已有研究表明,肿瘤细胞通过代谢产物、代谢酶和外切体的变化可以影响巨噬细胞表型和功能。肿瘤细胞衍生的琥珀酸通过激活巨噬细胞表面的琥珀酸受体来调节下游信号通路,以及肿瘤来源的外切体激活巨噬细胞中的信号通路,均促进巨噬细胞极化。因此,肿瘤细胞可能通过调节谷氨酰胺代谢影响巨噬细胞的表型,从而介导曲妥珠单抗耐药。
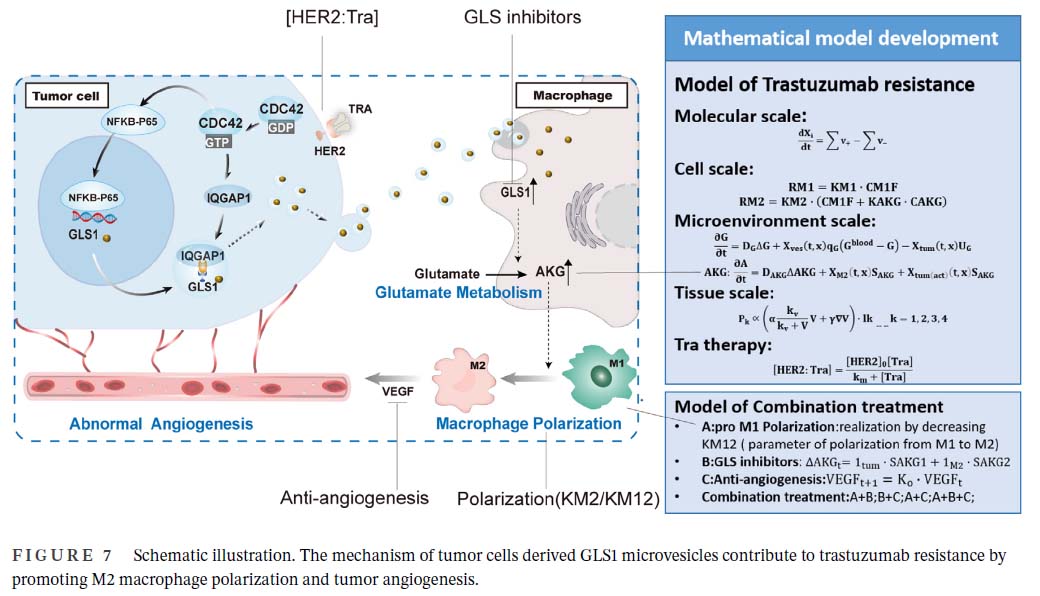
2023年7月11日,中山大学肿瘤防治中心王风华、南方医科大学石敏等研究团队在国际知名期刊Cancer Communications(IF=16.2)上发表了题为Glutamine metabolic microenvironment drives M2 macrophage polarization to mediate trastuzumab resistance in HER2-positive gastric cancer的文章。该研究主要针对谷氨酰胺代谢微环境驱动M2巨噬细胞极化,介导人HER2阳性胃癌研究,旨在进一步探讨曲妥珠单抗耐药的机制,以确定促进这些患者生存的治疗策略。
研究表明,肿瘤相关成纤维细胞可以产生和分泌谷氨酰胺,谷氨酰胺进入微环境促进肿瘤细胞的能量代谢,导致他莫昔芬耐药。也有学者研究得知,HER2阳性的乳腺癌有较高的谷氨酰胺代谢活性。因此,推测谷氨酰胺代谢与曲妥珠单抗耐药有关,靶向谷氨酰胺代谢可能是逆转曲妥珠单抗耐药性的有效策略。
该项研究主要研究了肿瘤细胞和巨噬细胞之间的代谢相互作用介导的曲妥珠单抗耐药。通过数学模型和动物实验探讨了联合治疗在逆转曲妥珠单抗耐药中的作用,所有与谷氨酰胺分解代谢相关的转运体和代谢酶都增加了,其中GLS1的表达最显著,且实验表明,阳性胃癌通过GLS1微泡促进M2巨噬细胞极化和血管生成,靶向谷氨酰胺代谢可以在体外和体内逆转曲妥珠单抗耐药。
该研究涉及的抗谷氨酰胺代谢、抗血管生成和M1极化治疗具有广阔的临床应用前景,有望以联合治疗的形式克服曲妥珠单抗耐药,成为HER2阳性进展期胃癌的一线治疗药物。
联科生物产品助力生命科学研究
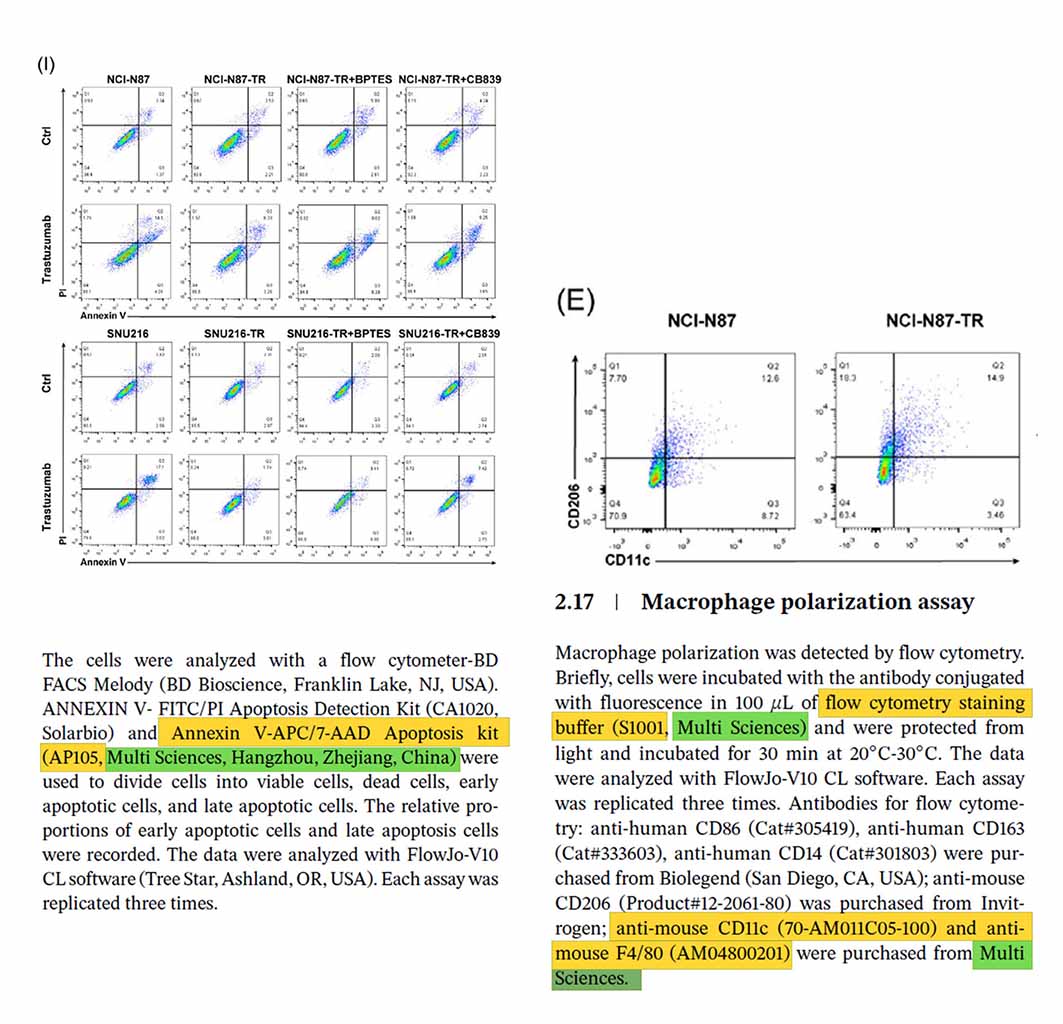
这篇论文使用了联科Annexin V-APC/7-AAD Apoptosis kit(AP105)、flow cytometry staining buffer(S1001)、anti-mouse CD11c,APC antibody(AM011C05)、anti-mouse F4/80,PE antibody(AM04800201)等产品。
凋亡试剂盒广泛应用于临床的科学研究,特别是疾病发生发展机制与靶向药物治疗上的研究,如肝癌、乳腺癌、肺癌、膀胱癌、卵巢癌等肿瘤疾病的靶向治疗手段中细胞的凋亡研究;甲状腺异常、系统性红斑狼疮、类风湿性关节炎等自身免疫性疾病发生发展机制研究;心肌缺血-再灌注损伤、心力衰竭、动脉粥样硬化等心血管疾病发展及预后研究;再生障碍性贫血等血液性疾病的治疗研究;阿尔兹海默病、帕金森综合征等神经退行性疾病长期监测研究。
流式staining buffer在流式检测中是必不可少的辅助试剂,专业的流式染色缓冲液非常适用于单细胞的流式检测,既能保证细胞的活性又含可以最大程度的减少抗体非特异性结合,提升流式检测结果图形的准确性与美观度。
CD11c与F4/80则是小鼠巨噬细胞检测中的必测指标。巨噬细胞的检测通常出现在癌症、自身免疫性疾病、感染疾病、血液病等临床科研研究中,主要通过小鼠造模等方式,对小鼠模型的血液、实体肿瘤、脾脏等组织细胞进行具体的免疫评估并分析,帮助了解其生理、病理过程中的作用。
| 货号 | 产品名 | 部分引用文献 |
| AP105 | Annexin V-APC/7-AAD Apoptosis kit | Spleen fibroblastic reticular cell-derived acetylcholine promotes lipid metabolism to drive autoreactive B cell responses |
| miR-448 targets IDO1 and regulates CD8 + T cell response in human colon cancer | ||
| CDK4/6 inhibition enhances oncolytic virus efficacy by potentiating tumor-selective cell killing and T cell activation in refractory glioblastoma | ||
| Ferritin Nanocaged Doxorubicin Potentiates Chemo-Immunotherapy against Hepatocellular Carcinoma via Immunogenic Cell Death | ||
| S1001 | flow cytometry staining buffer | Sulfonium-Driven Neoantigen-Released DNA Nanodevice as a Precise Vaccine for Tumor Immunotherapy and Prevention |
| Changes in the balance of Th17/Treg cells and oxidative stress markers in patients with HIV‑associated pulmonary tuberculosis who develop IRIS | ||
| Blocking the IFN-gamma signal in the choroid plexus confers resistance to experimental autoimmune encephalomyelitis | ||
| Multifunctional magnesium-organic framework doped biodegradable bone cement for antibacterial growth, inflammatory regulation and osteogenic differentiation | ||
| AM011C05 | anti-mouse CD11c,APC antibody | High baseline tumor burden-associated macrophages promote an immunosuppressive microenvironment and reduce the efficacy of immune checkpoint |
| Remodeling Chondroitin-6-Sulfate–Mediated Immune Exclusion Enhances Anti–PD-1 Response in Colorectal Cancer with Microsatellite Stability | ||
| Deficiency of eIF4B Increases Mouse Mortality and Impairs Antiviral Immunity | ||
| AM04800201 | anti-mouse F4/80, PE antibody | Bioengineered Nanospores Selectively Blocking LC3-Associated Phagocytosis in Tumor-Associated Macrophages Potentiate Antitumor Immunity |
| Engineering nanoparticles boost TNBC therapy by CD24 blockade and mitochondrial dynamics regulation | ||
| Polyguanine alleviated autoimmune hepatitis through regulation of macrophage receptor with collagenous structure and TLR4-TRIF-NF-κB signalling |
参考文献:
Xingbin Hu, Wangjun Liao, Fenghua Wang, Min Shi, et al.Glutamine metabolic microenvironment drives M2 macrophage polarization tomediate trastuzumab resistance in HER2-positive gastric cancer.Cancer Communications, 2023;43:909–937.
原文链接:
https://onlinelibrary.wiley.com/doi/abs/10.1002/cac2.12459