即使在氧气充足的情况下,癌细胞也倾向于通过厌氧糖酵解来满足其能量需求,从而产生大量的乳酸,这被称为“瓦堡效应”。 为了维持细胞内稳态,癌细胞会排出乳酸,导致肿瘤微环境(tumor microenvironment,TME)酸化,这与肿瘤的侵袭、转移以及对化疗、免疫治疗等治疗的抵抗密切相关。这种酸性的TME被认为对淋巴细胞有毒性,导致增殖抑制和细胞毒性。pH降至6.0 ~ 6.5足以使人和小鼠的肿瘤特异性CD8+ T细胞失活,并伴有细胞溶解能力和细胞因子分泌受损,IL-2Rα (CD25)和T细胞受体(TCR)表达降低,信号转导因子和激活因子5和细胞外信号调节激酶的激活降低。此外,这种酸性环境还会作用于自然杀伤细胞(NK)和巨噬细胞,加重免疫抑制的TME。因此,中和酸性的TME可以为肿瘤的免疫治疗提供环境基础,挽救失活的免疫细胞。
来自浙江大学药学院的研究团队在期刊《ACS NANO》上发表了题为Arginine Supplementation Targeting Tumor-Killing Immune Cells Reconstructs the Tumor Microenvironment and Enhances the Antitumor的学术论文,他们尝试在L -精氨酸补充过程中保持肿瘤饥饿状态,以促进肿瘤免疫治疗的敏化,阐明微环境、营养和代谢在肿瘤治疗中的重要性,为重建微环境拯救肿瘤中失活的免疫细胞提供参考。
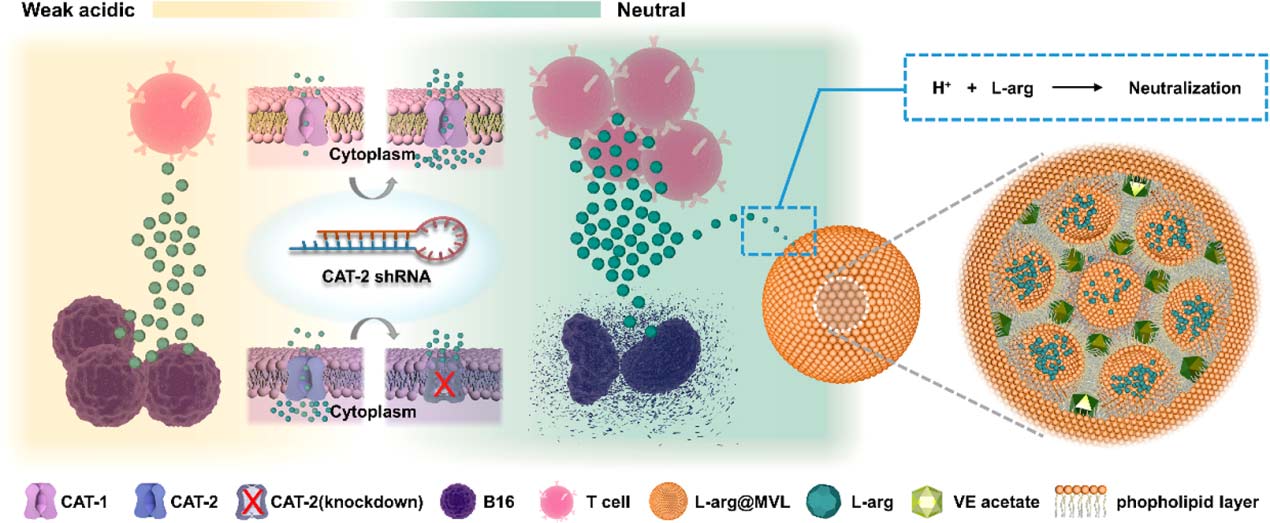
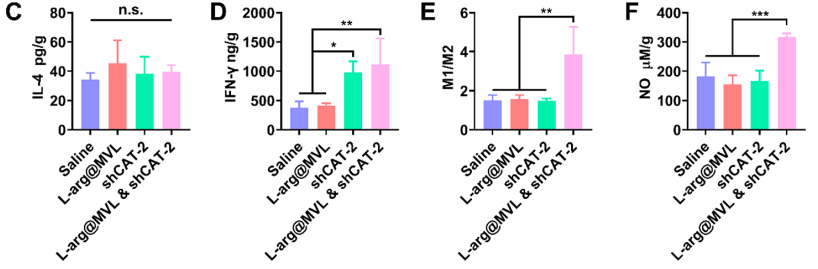
研究团队制备了微米级多腔多泡脂质体包封L-精氨酸(L-arg@MVLs),实现高效包封和缓释。体外研究发现CD8+ T细胞和M1巨噬细胞更依赖于CAT-1摄取L-精氨酸,而黑色素瘤细胞和M2巨噬细胞更倾向于使用CAT-2。根据L -精氨酸的碱度保留,他们推测瘤内注射L-arg@MVLs可以持续中和弱酸,并在TME中供应L-精氨酸,从而为抗肿瘤免疫细胞提供合适的生存环境和足够的营养支持。同时,利用短发夹RNA下调肿瘤组织中CAT-2的表达,防止癌细胞从充足的L-精氨酸中获益。该研究团队的策略表现出良好的免疫促进功能,通过调节酸性TME和营养代谢抑制黑色素瘤生长,并增强了肿瘤对免疫检查点抑制剂(ICB)治疗的反应。
MULTISCIENCES 产品支撑
Mouse IFN-γ ELISA Kit(EK280/3)

-
- EK280 477 Citations
- ELISA试剂盒
Mouse IFN-gamma ELISA Kit检测试剂盒(酶联免疫吸附法)
- ¥1,600.00 – ¥10,800.00